2019-05-19 07:39:00 来源:
本周(5月12日至18日)行业政策方面,国家药监局就三个关于药品追溯方面的文件向社会公开征求意见。企业层面,证监会通报康美药业(600518.SH)调查进展,公司2016至2018年财务报告存在重大虚假,股票将于5月21日被实施ST;吉药控股(300108.SZ)实控人将变更为吉林省国资委;仙琚制药(002332.SZ)陷药品“回扣门”事件;通化金马(000766.SZ)和澳洋健康(002172.SZ)布局工业大麻。研发层面,3个国家1类新药获批临床试验,3家企业产品获批注册,海正药业(600267.SH)制剂获批在美上市。
5月16日,国家药监局发布公开公告称,将对近期完成的《疫苗追溯基本数据集(征求意见稿)》《疫苗追溯数据交换基本技术要求(征求意见稿)》和《药品追溯系统基本技术要求(征求意见稿)》公开征求意见,截止时间为6月15日。
5月13日,国家卫健委、国家发改委等5部门联合发布《关于开展促进诊所发展试点的意见》,称2019到2020年将在北京、上海、沈阳等10个城市开展促进诊所发展试点工作,从简化准入程序、调整设置标准、激发存量活力、创新监管手段等方面提出要求。
5月13日,财政部发布公告称,根据《中华人民共和国对外贸易法》《中华人民共和国进出口关税条例》等法律法规和国际法基本原则,国务院关税税则委员会决定,自2019年6月1日0时起,对原产于美国的部分进口商品提高加征关税税率。根据公告及附件,此次加征关税商品包含了重组人胰岛素及其盐、血压测试仪器及器具、布洛芬、B型超声波诊断仪、彩色超声波诊断仪等大批药品、医疗器械产品。

5月17日,证监会通报对康美药业(600518.SH)的调查进展,初步查明康美药业披露的2016至2018年财务报告存在重大虚假,涉嫌违反《证券法》第63条等相关规定。一是使用虚假银行单据虚增存款,二是通过伪造业务凭证进行收入造假,三是部分资金转入关联方账户买卖本公司股票。此前证监会也已对公司审计机构正中珠江会计师事务所涉嫌未勤勉尽责立案调查。有关案件进展情况,证监会将及时向社会公布。
5月17日晚,康美药业发布公告称,公司与相关关联公司存在88.79亿元的资金往来,该等资金被相关关联公司用于购买公司股票,行为触及《上海证券交易所股票上市规则》13.1.1条规定“投资者难以判断公司前景,投资者权益可能受到损害”的情形。公司股票申请5月20日停牌1天,将于5月21日恢复交易,并实施其他风险警示,股票简称变更为ST康美。
公司还称,经自查,因公司治理、内部控制存在缺陷,资金管理、关联交易管理等方面存在重大缺陷,违反了公司日常资金管理规范及关联交易管理制度的相关规定。公司将督促相关关联公司通过多种途径解决资金往来的问题,消除相关影响,挽回损失。
此前的5月12日,公司收到年报问询函,要求公司从业务板块及毛利率、资产及负债项目、业绩和现金流等方面做出补充披露。5月13日晚,公司称申请延期回复4月30日和5月5日分别收到的监管工作函和问询函,回复时间将不晚于5月21日。
简评:自4月30日康美药业发布财务差错更正导致近300亿货币资金“不翼而飞”受到市场高度关注,其股价走出6个跌停,市值一度蒸发达260亿元,但近期连续拉出阳线,甚至在5月16日涨停。此番证监会通报的调查进展基本坐实公司财务造假行为,且其还涉嫌通过关联资金“坐庄”自家股票,打脸公司董事长马兴田此前“财务差错和财务造假是两回事”的回应。随着公司回复函件,具体造假行为或将进一步曝光。在5月21日被实施ST后,该股恐怕将会再次承压,不排除多个跌停可能。
5月17日,吉药控股(300108.SZ)称,控股股东卢忠奎和黄克凤夫妇,以及股东孙军和梅河口金河德正创业投资中心(有限合伙)与吉林省吉盛资产管理有限责任公司(下称吉盛资产)签署了股份转让意向协议,前述股东拟合计转让15.18%的股份给吉盛资产,其中卢忠奎和黄克凤还将剩余持有14.29%的股份所对应的表决权等委托给吉盛资产。此次交易完成后,吉盛资产将成为吉药控股的控股股东,吉林省国资委将成为实控人。
简评:这是在不到两周的时间,第三家计划易主国资平台的民营上市药企。目前此次股份转让价格、交易方式和支付方式均尚未确定,按照协议签署前一交易日5月16日6.78元/股的收盘价计,此次股份转让款合计接近6.85亿元。此次计划转让的股东均面临高质押而导致的债务压力,且公司盈利最近两年持续承压,或是其选择易主国资平台的主因。
5月17日,仙琚制药(002332.SZ)发布说明公告,公司产品糠酸莫米松鼻喷雾剂通过代理模式进行销售,在江苏省由代理商全权负责进行终端学术推广和销售,公司与代理商是两个不同的法律主体。该产品2018年在江苏省的销售金额约为人民币280余万元。公司关注到该事项后已及时与相关部门及代理商取得联系,主动予以配合。若相关方存在违规行为,公司亦将进行严肃处理。
此前江苏省卫健委下发函件称,收到实名举报,反映仙琚制药为扩大其产品糠酸莫米松鼻喷雾剂(50μg,60揿/盒)销量,给江苏省部分医疗机构医生15元/盒回扣。江苏省卫健委要求各设区市卫生健康委医政处、行风办认真核查,核查结果于5月31日前上报。
简评:受“回扣门”事件影响,仙琚制药股价在5月16日和17日连续下跌。此次涉事的产品糠酸莫米松鼻喷雾剂是公司于2011年12月获批上市的国产独家仿制药,属于过敏性鼻炎的一线治疗药物,自被纳入2017年新版国家医保目录(乙类)后快速放量,去年市场份额达到23%,但与原研厂家默沙东旗下的先灵葆雅仍有较大差距。在行业不断整治医药贿赂和回扣行为的政策环境下,若后续查证属实,涉事单位或人员或面临一定处罚,公司产品口碑和销售恐也会受到一定影响。
5月17日晚,昭衍新药(603127.SH)称,公司拟通过在美国设立特殊目的公司以2728万美元(约合人民币1.89亿元)收购美国企业BIOMEDICAL RESEARCH MODELS, INC.100%股权。标的公司创立于1996年12月,系一家临床前CRO公司,业务包括临床前CRO业务和疫苗研发业务,其中疫苗业务会在交割前剥离。
简评:目标公司去年CRO业务实现营收1.26亿元,净利润0.11亿元,而此次收购价格相较其剥离疫苗资产后的净资产溢价高达超过13倍,收购完成将形成较多商誉。目标公司的CRO业务与昭衍新药基本相同,均为临床前CRO业务,具有较强的业务协同和技术协同,公司也将借此拓展美国市场,积累海外并购经验。此次收购还需相关部门批准,存在一定审批风险。
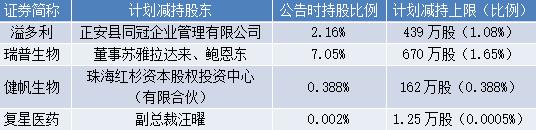
本周溢多利(300381.SZ)、瑞普生物(300119.SZ)、健帆生物(300529.SZ)、复星医药(600196.SH)等企业股东计划减持,其中健帆生物的股东珠海红杉资本股权投资中心(有限合伙)计划清仓减持,该股东自去年11月至今年5月已合计减持近622万股(占公司总股本的1.49%),另瑞普生物的两名董事、复星医药的副总裁汪曜也计划减持。
5月16日晚,万东医疗(600055.SH)称,杭州裕桦投资合伙企业(有限合伙)、上海盛宇股权投资基金管理有限公司对公司控股子公司万里云医疗信息科技(北京)有限公司(下称万里云)各自增资5000万元,此次交易各方按万里云投后估值14.50亿元为定价依据。此次增持前,万东医疗和阿里健康分别持有万里云75%和25%的股权,增资后万东医疗和阿里健康持股比例分别降至55.86%和23.28%,两名新股东均持股3.45%,员工持股平台持股13.96%。
5月14日晚,通化金马(000766.SZ)称,公司与黑龙江省七台河市政府、黑龙江省科学院共同签署工业大麻合作项目协议,拓展公司在工业大麻领域的育种、种植、提取、深加工方面的深度开发,实施工业大麻科技成果研发与转化。本次合作期限为五年,公司需向黑龙江省科学院及其所属大庆分院共支付1500万元研发经费。通化金马此前已多次布局工业大麻,包括与吉林省农科院前述项目协议、成立两家子公司等,包括此次在内累计投资金额已达6300万元。
5月13日晚,澳洋健康(002172.SZ)称,控股子公司阜宁澳洋科技有限责任公司与江苏省纺织工业设计研究院有限公司、黑龙江省赵光农场签订了战略合作协议,分别就工业大麻纤维生产及技术研发、工业大麻的种植及麻皮收购等事宜达成合作。5月14日,公司股价涨停,同时收到深交所关注函,要求公司说明合作事项的可行性、关联性、是否存在利用工业大麻概念炒作股价配合股东减持情形。
5月13日晚,常山药业(300255.SZ)称,高树华由于个人原因申请辞去公司董事长、总经理职务,一并辞去公司董事及董事会各专门委员会职务,辞职后高树华将不担任公司任何职务。
本周舒泰神(300204.SZ)、天士力(600535.SH)、康缘药业(600557.SH)、安科生物(300009.SZ)、恒瑞医药(600276.SH)等企业产品在临床初期获得进展,其中舒泰神用于治疗血友病的凝血因子X激活剂的临床申请获得国家药监局受理,该产品系国家1类治疗用生物制品。

另外4家企业产品均获得临床试验通知书,其中天士力用于治疗Ⅱ型糖尿病的TSL-0319胶囊及康缘药业和中国科学院上海药物研究所联合申报用于治疗良性前列腺增生的喹诺利辛片均属于国家1类化学药;恒瑞医药用于难治性抑郁症治疗的盐酸(R)-氯胺酮鼻喷剂在国内尚无同类产品上市,但有同类产品处于临床,国外杨森制药有同类产品获批在美国上市。
本周新华制药(000756.SZ)、康弘药业(002773.SZ)、京新药业(002020.SZ)等三家企业收到国家药监局下发的药品注册批件,其中康弘药业的国家1类生物创新药康柏西普眼用注射液此次获批新增的适应症为糖尿病性黄斑水肿引起的视力损害,该产品2013年获批用于治疗湿性年龄相关性黄斑变性,2017年获批用于治疗继发于病理性近视脉络膜新生血管引起的视力损伤。

5月15日晚,海正药业(600267.SH)称,控股子公司海正药业(杭州)有限公司申报的注射用盐酸多柔比星的ANDA(即美国仿制药申请)获得美国FDA批准。该产品主要适用于乳腺癌术后辅助治疗、其他恶性肿瘤病的治疗,国内外厂商主要有WEST-WARD PHARMS INT、AMNEAL PHARMS、深圳万乐药业、山西普德药业等。该产品2018年全球销售额约5.73亿美元,其中美国市场约1.64亿美元。
免责声明:本网站所有信息仅供参考,不做交易和服务的根据,如自行使用本网资料发生偏差,本站概不负责,亦不负任何法律责任。如有侵权行为,请第一时间联系我们修改或删除,多谢。

© 2018 今日中国财经 版权所有