2019-04-07 12:36:00 来源:
本周(3月31日至4月6日)政策方面,医疗器械临床试验审批也进入默示许可制时代。本周仅有13家药企发布年报,智飞生物(300122.SZ)业绩翻倍,独家产品暂停生产致股价大跌;通化金马(000766.SZ)和福安药业(300194.SZ)涉足工业大麻,引发深交所炒作股价的质问。另有7家药企股东计划减持,平安方面计划减持云南白药(000538.SZ)3%股份,华大基因(300676.SH)被查出三大问题要求被整改。研发层面,人福医药(600079.SH)、华东医药(000963.SZ)、通化东宝(600867.SH)取得进展。
4月4日,国家药监局发布公告,注销85个药品批准文号,其中53个是由于企业主动申请,13个是因已撤销药品批准证明文件,另外19个药品批准文号被注销是由于企业被依法吊销《药品生产许可证》,而这19个被被注销的批准文号均来自处于退市倒计时的长生生物(002680.SZ)旗下的长春长生生物科技有限责任公司,注销产品包括此前涉事的狂犬病疫苗、百白破疫苗等18个疫苗产品和胸腺肽注射液。
4月4日,国家药监局再次公开征求《关于进一步完善药品关联审评审批和监管工作有关事宜的公告(征求意见稿)》意见,进一步明确原料药、药用辅料、药包材与药品关联审评审批和监管有关事宜,其中提出对仿制国内已上市的原料药,登记时可以不与药品制剂关联,即单独登记,经审评通过后,登记状态标识为“A”,不再发给药品批准文号;药用辅料、药包材已取消行政许可,平台登记不收取费用。
原料药企业的审批制度造成了批文的稀缺性,在一定程度上也助推了原料药价格上涨,甚至垄断。原料药批文取消,或将推动原料药市场竞争更加激烈,这也被业内视为国家打破原料药价格垄断的重要举措。
4月1日,国家药监局发布关于调整医疗器械临床试验审批程序的公告,提出自临床试验审批申请受理并缴费之日起60个工作日内,申请人在预留联系方式、邮寄地址有效的前提下,未收到国家药监局器审中心意见(包括专家咨询会议通知和补充资料通知)的可以开展临床试验;同意开展临床试验的,审查结果将通过器审中心网站告知申请人,不再发放临床试验批件。这意味着,自去年7月国家药监局推出药物临床试验默示许可制后,该方式又拓展至医疗器械,审批程序进一步优化。
本周仅有13家药企发布2018年年报,其中天坛生物(600161.SH)、红日药业(300026.SZ)、广生堂(300436.SZ)、吉林敖东(000623.SZ)、亿帆医药(002019.SZ)5家企业净利润出现不同程度下降。
在8家净利润出现增长的企业中,智飞生物(300122.SZ)增长最为强劲。根据4月3日晚该公司发布的年报,去年实现营收52.28亿元,同比增长289%;净利润14.51亿元,同比增长236%。该公司拟每10股派发5元,合计分红8亿元。
智飞生物目前共有5种自主产品和6种代理或协议推广产品在售,其中全球独家品种AC-Hib三联疫苗和代理的默沙东HPV疫苗是公司业绩的核心推动力。
去年智飞生物自主产品疫苗收入12.42亿元,同比增长近26%,占公司营收的比重从上年的74%左右大幅下降至24%,但其毛利率仍维持在高位,达到95.42%。其中AC-Hib三联疫苗是自主产品的核心,去年其批签发近644万支,同比增长约37%,是公司批签发量最多的品种。光大证券预计AC-Hib三联疫苗去年销售550万支,贡献收入超11亿元,同比增长38%。
值得注意的是,AC-Hib三联疫苗面临暂停生产。4月1日晚智飞生物发布公告称,去年11月向北京市食药监局提交AC-Hib三联疫苗再注册申请,目前行政程序尚未完成,公司尚未收到再注册批件。鉴于原药品批准文号有效期至2019年4月1日,因此在未获得再注册批件之前将暂停AC-Hib三联疫苗生产。
这直接导致4月2日智飞生物跌停,单日市值蒸发近83元;4月4日,在业绩大幅增长的情况下,该股仍大跌4.73%,市场担忧情绪明显。智飞生物称,若AC-Hib三联疫苗不再获批注册,将对公司2019年及今后的经营业绩产生较大影响,其在回应媒体时称此次并不涉及AC-Hib三联疫苗的产品质量问题,且还有一定库存。
据中泰证券研报,目前智飞生物生产有600万支左右AC-Hib三联疫苗(原生产批件有效期内生产),后续有望陆续批签发,基本可以满足一年左右需求。按中性预期该产品在2019年获得再注册批件,则对2019-2020业绩没有影响;若悲观预期则再注册无法获得批件,新的三联苗冻干剂型有望于2020年底获批,则三联苗缺货0.5-1年,对2020年净利润有一定影响。
代理产品则成为智飞生物业绩贡献的第一大主力,去年实现收入38.88亿元,同比大幅增长1319%,对公司营收的贡献从上年的20%大幅增加至74%,同时其毛利率也增长近12个百分点达到41.28%。这主要系公司代理的默沙东的四价HPV疫苗、九价HPV疫苗迅速放量所致,去年批签发量分别为380万支、122万支,其中四价HPV疫苗同比增长992%。
2018年11月5日,智飞生物与默沙东就四价和九价HPV疫苗约定了自2019年至2021年6月30日期间共计约180.02亿元的产品基础采购金额。若AC-Hib三联疫苗无法及时再获批生产,HPV疫苗将成为业绩核心增长点,有望填补一定业绩空缺。
3月31日晚,通化金马(000766.SZ)称,公司与吉林省农科院、通化市二道江区人民政府共同签署《工业大麻合作项目协议》,探索工业大麻育种、种植及研发。合作期限五年,公司将分期支付研发经费,研发经费总额约3838万元。深交所4月1日下发关注函,要求公司说明开展工业大麻的必要性、相关资质、技术与人才储备,以及是否存在主动迎合市场热点、炒作股价、配合股东减持的情形。
4月1日,福安药业(300194.SZ)称,公司与在美国内华达州拉斯维加斯拥有成熟的工业大麻种植基地、加工设备和销售渠道的两家企业Red Realty LLC、Golden Way Investor, LLC签订了《合作意向协议》,拟利用各自优势在工业大麻绿色种植,工业大麻产品提取、深加工等领域开展合作。当日深交所下发问询函,要求公司说明是否涉嫌炒作股价、合作必要性、可行性和发展前景、是否具备技术与人才储备、合作对方情况等。
4月3日,继在3月28日签订合作框架协议后,华仁药业(300110.SZ)公布具体合作方式,公司与云南素麻、侯杰计划共同设立合资公司,合作在云南建设工业大麻绿色工厂,打造中国第一家工业大麻温室大棚种植基地。合资公司注册资本约为1.33亿元,公司现金出资持股45%,云南素麻以种植技术及相关资质评估作价方式出资持股35%。
简评:这三家企业因工业大麻本周股价上涨明显,业绩巨亏的福安药业更是连续拉出五个涨停,而通化金马得控股股东及其一致行动人此前计划减持不超过10%股份,也被深交所质问是否存在配合股东减持情况,华仁药业两大股东在4月2日晚称合计减持不超过4%股份,但市场不惧减持继续推动该股上涨。目前计划布局工业大麻的企业几乎都还未实际开展业务,近期多个部门也要求加强工业大麻审批和管理,工业大麻概念股表现受到一定程度打击,后续仍存在诸多风险。
4月4日晚,亚宝药业(600351.SH)称,控股股东山西亚宝投资集团有限公司(下称亚宝投资)将其持有的公司6300万股无限售流通股(占总股份的8.18%)转让给广东晋亚纾困股权投资合伙企业(有限合伙)(下称晋亚纾困),晋亚纾困将上述股份的表决权、提案权及参加股东大会的权利委托给亚宝投资全权行使。此次股份转让价格为7.4元/股,转让价款合计为4.66亿元。
简评:亚宝投资此次转让股份是为了纾解资金的暂时流动性困难,而晋亚纾困是山西国投旗下企业,亚宝药业则是继东杰智能、振东制药后山西第三家被地方国资背景企业纾困的A股公司。但有所不同的是,此次晋亚纾困将标的股份表决权等仍交由亚宝投资行使,仅要求未来董事会换届提名一名非独立董事。此次转让完成后,亚宝投资持有公司17.13%股份,仍为控股股东。
本周浙江医药(600216.SH)、药石科技(300725.SZ)、盘龙药业(002864.SZ)、华仁药业(300110.SZ)、云南白药(000538.SZ)、葵花药业(002737.SZ)、复旦复华(600624.SH)等7家企业股东计划减持,其中引发市场关注的是云南白药持股9.40%的第三大股东中国平安人寿保险股份有限公司(下称平安人寿)计划减持不超过3124万股(占总股本的3%),减持原因为系资金周转需要。4月3日午间云南白药发布该消息后,其股价午后开盘大幅下挫,跌幅一度超过3%。
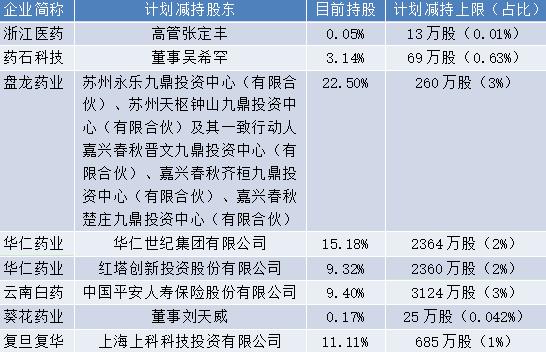
平安人寿于2008年以近14亿元通过定增成为云南白药重要股东,该项投资已浮盈数倍,而其在去年8月就已发布过减持计划,但最终未减持,此次则是延续。值得注意的是,该股东代表董事还在云南白药吸收合并控股股东事项中投出唯一的反对票,且公司业绩持续疲软,继续推进减持或反映出平安方面对云南白药未来预期有所降低,平安集团则回应称此次减持系其整体投资组合再平衡和动态调整的一部分。按最新股价和减持上限计,平安人寿此次有望套现约27亿元。
4月4日晚,华大基因(300676.SH)称,收到中国证监会深圳监管局下发的责令改正措施的决定。经检查发现,公司主要存在三大问题:一是存在订单型收入确认依赖的系统存在漏洞,因跨期撤销交付并导致相关收入成本核算跨期问题,使得公司2017年少计收入50万元、净利润42万元;同时存在样本编码重复并导致收入重复核算问题,使得公司2017年多计收入38万元、净利润32万元。
二是部分项目型收入核算与会计政策不一致,公司2017年多计收入1328万元、净利润1245万元。三是规范运作程度不高,存在部分执行的财务制度不规范、关联方员工参与公司项目工作、向关联方华大智造预付款超过合同约定(多支付0.31亿元)等情形。深圳监管局要求公司责令改正,并对实控人及董事长汪建、总经理尹烨和财务总监陈轶青出具警示函。
4月3日晚,江中药业(600750.SH)称,华润医药控股对公司发起的要约收购期限届满,在3月4日起至4月2日要约收购期间,公司股东预受要约股份共计816,175股,撤回预受要约股份共计801,518股,最终有17个账户共计14,657股股份接受收购人发出的要约。
4月1日晚,海思科(002653.SZ)称,公司全资子公司四川海思科与美国公司eXIthera签署《股权认购协议》及《独家许可协议》,拟使用600万美元认购eXIthera发行的278.71万股普通股,并获得其产品EP-7041在中国境内的独家许可。该产品已在澳洲完成Ⅰ期临床并即将在美国递交临床申请,有望成为抗凝血和抗血栓药物市场的主流药物。
4月3日晚,人福医药(600079.SH)称,控股子公司宜昌人福药业有限责任公司收到国家药监局核准签发的盐酸安非他酮缓释片的临床试验通知书,豁免药代动力学试验。该产品适用于治疗中重度抑郁症以及季节性情感障碍,去年6月获得美国FDA批准文号
4月3日晚,华东医药(000963.SZ)称,公司全资子公司杭州中美华东制药有限公司向美国FDA申报的注射用泮托拉唑钠冻干粉针无菌注射剂的ANDA(即美国仿制药申请)已获得暂时批准(指美国FDA已经完成该药品的所有审评流程,但存在相关专利未到期的情形)。该产品主要适用于急性上消化道出血,目前美国境内厂商仅为原研公司日本武田制药。
4月2日晚,通化东宝(600867.SH)称,收到西格列汀二甲双胍片(Ⅱ)药品注册申请受理通知书。该产品由默沙东原研开发,2007年3月在美国上市,用于Ⅱ型糖尿病的口服治疗,次年在欧盟获批上市,2012年我国批准进口。目前国内未有仿制药品批准上市,有2家厂家对该药品进行了申报生产注册。
免责声明:本网站所有信息仅供参考,不做交易和服务的根据,如自行使用本网资料发生偏差,本站概不负责,亦不负任何法律责任。如有侵权行为,请第一时间联系我们修改或删除,多谢。

© 2018 今日中国财经 版权所有